Para medir el el diámetro corneal
La topografía corneal es una herramienta diagnóstica computerizada que crea un mapa tridimensional de la superficie curva de la córnea. La córnea es la parte transparente más externa del ojo que tiene forma de bóveda y cuyo tamaño es similar al diámetro del iris (zona coloreada del ojo). La gran ventaja de la topografía corneal sobre otros métodos es su facilidad para detectar irregularidades corneales invisibles por medio de la mayoría de los exámenes convencionales.
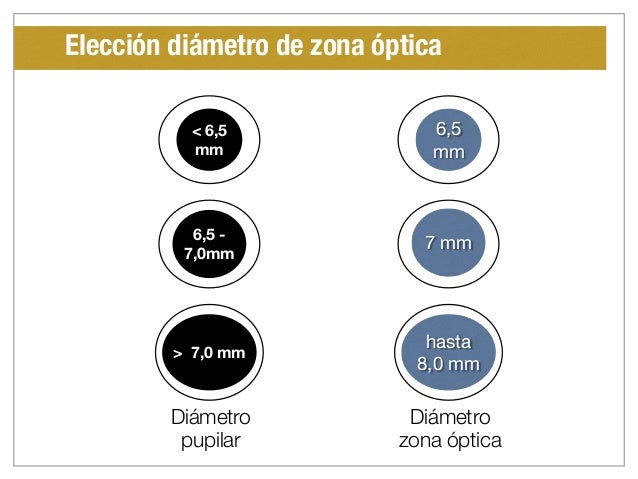
Para medir el diámetro pupilar
La pupila natural del ojo humano suele ser aproximadamente circular y, en determinadas condiciones externas, su diámetro depende del sujeto y de su estado psicofísico. Para un dado sujeto, el patrón de aberraciones, la difracción, la profundidad de campo y la iluminación retiniana dependen del diámetro pupilar, el cual a su vez varía en función de la iluminación ambiente. El conocimiento de este diámetro es importante tanto en pruebas objetivas como subjetivas en las cuales se determina la calidad visual. La medición del diámetro pupilar también se utiliza como indicador del nivel de vigilia o anestesia o para detectar la presencia de narcóticos. En este trabajo se presenta un software desarrollado en MATLAB (denominado AS08) capaz de procesar imágenes y de medir el diámetro de una pupila circular. Se consideran imágenes registradas dentro del espectro visible y también en el infrarrojo cercano. En el software AS08 se utilizan varias técnicas de procesamiento de imágenes, entre las cuales cabe destacar la transformada de Hough, por sus conocidas virtudes referentes al reducido consumo de recursos computacionales para detectar círculos.
Apertura palpebral
En reposo, el párpado superior suele cubrir aproximadamente 2mm del iris, en cambio, el párpado inferior no suele sobrepasar el limbo inferior, siendo su velocidad media 18 parpadeos/minuto. Su correcta exploración debe incluir además su posición en todas las direcciones de la mirada y en cierre/apertura máxima voluntaria.
-Consideramos que existe un ptosis palpebral cuando la superficie cubierta es mayor, llegando incluso al borde superior de la pupila e independientemente de la causa. Al contrario, cuando existe una anomalía en el cierre, la longitud de la hendidura palpebral es mayor en el ojo afecto. En el diagnóstico diferencial de dichos trastornos debe incluir problemas mecánicos locales, enfermedades musculares , o de la unión neuromuscular, patología a nivel del nervio periférico o a nivel central.
La existencia de una ptosis, se suele acompañar de una elevación compensatoria de la cabeza y contracción de musculatura frontal para vencer el déficit visual secundario. La ptosis o “caída palpebral” no es infrecuente en la población anciana como consecuencia de la hiperlaxitud tarsal, pudiéndose presentar de forma uni o bilateral. Entre las causa más comunes, hay que diferenciarla de la apraxia de la apertura palpebral, en la cual existe imposibilidad para la apertura de forma voluntaria, pudiéndose llevar a cabo, en cambio, espontáneamente, así como de la lesión del III par craneal, en la cual además encontraremos anomalías pupilares y/o de la motilidad ocular, y de la ptosis secundaria a lesión a nivel de la vía simpática (Síndrome de Horner). Otra patología frecuente que no hay que olvidar es la ptosis secundaria a la Miastenia Gravis, que característicamente cursa de forma fluctuante, o en el contexto de una miopatía u otras patologías miasteniformes, en cuyo caso debemos buscar afectación a otros niveles.
-El cierre palpebral excesivo generalmente lo encontramos de forma secundaria a blefaroespasmo (contracción involuntaria de la musculatura orbicular), hemiespasmo facial, (contracción involuntaria de toda la musculatura inervada por el VII Par ipsilateral) o la apraxia , de la apertura palpebral (incapacidad para la apertura de forma voluntaria, pudiéndose realizar correctamente de forma espontánea).En otras causas de cierre palpebral excesivo, como la miotonía, se suelen objetivar alteraciones en la exploración física también a otros niveles.
-El defecto del cierre palpebral suele estar en relación con un parpadeo incompleto en el cual se deja en exposición la superficie corneal (secundario a proptosis, paresia del VII Par, etc…). La existencia de “retracción” palpebral, incluye la exposición de la esclera, en reposo, entre el limbo corneal y el límite palpebral, de forma dinámica, se objetiva un retraso en el movimiento palpebral el cual podemos poner de manifiesto haciendo fijar la mirada en un objeto que se desplace forzando la mirada inferior, y generalmente se relaciona con la oftalmopatía tiroidea.
-Consideramos que existe un ptosis palpebral cuando la superficie cubierta es mayor, llegando incluso al borde superior de la pupila e independientemente de la causa. Al contrario, cuando existe una anomalía en el cierre, la longitud de la hendidura palpebral es mayor en el ojo afecto. En el diagnóstico diferencial de dichos trastornos debe incluir problemas mecánicos locales, enfermedades musculares , o de la unión neuromuscular, patología a nivel del nervio periférico o a nivel central.
La existencia de una ptosis, se suele acompañar de una elevación compensatoria de la cabeza y contracción de musculatura frontal para vencer el déficit visual secundario. La ptosis o “caída palpebral” no es infrecuente en la población anciana como consecuencia de la hiperlaxitud tarsal, pudiéndose presentar de forma uni o bilateral. Entre las causa más comunes, hay que diferenciarla de la apraxia de la apertura palpebral, en la cual existe imposibilidad para la apertura de forma voluntaria, pudiéndose llevar a cabo, en cambio, espontáneamente, así como de la lesión del III par craneal, en la cual además encontraremos anomalías pupilares y/o de la motilidad ocular, y de la ptosis secundaria a lesión a nivel de la vía simpática (Síndrome de Horner). Otra patología frecuente que no hay que olvidar es la ptosis secundaria a la Miastenia Gravis, que característicamente cursa de forma fluctuante, o en el contexto de una miopatía u otras patologías miasteniformes, en cuyo caso debemos buscar afectación a otros niveles.
-El cierre palpebral excesivo generalmente lo encontramos de forma secundaria a blefaroespasmo (contracción involuntaria de la musculatura orbicular), hemiespasmo facial, (contracción involuntaria de toda la musculatura inervada por el VII Par ipsilateral) o la apraxia , de la apertura palpebral (incapacidad para la apertura de forma voluntaria, pudiéndose realizar correctamente de forma espontánea).En otras causas de cierre palpebral excesivo, como la miotonía, se suelen objetivar alteraciones en la exploración física también a otros niveles.
-El defecto del cierre palpebral suele estar en relación con un parpadeo incompleto en el cual se deja en exposición la superficie corneal (secundario a proptosis, paresia del VII Par, etc…). La existencia de “retracción” palpebral, incluye la exposición de la esclera, en reposo, entre el limbo corneal y el límite palpebral, de forma dinámica, se objetiva un retraso en el movimiento palpebral el cual podemos poner de manifiesto haciendo fijar la mirada en un objeto que se desplace forzando la mirada inferior, y generalmente se relaciona con la oftalmopatía tiroidea.
MEDICIÓN DE LA POSICIÓN DE LOS PÁRPADOS
|
Altura de la Fisura Interpalpebral
1. Pedir al paciente que fije la mirada hacia la luz de la linterna, en la posición primaria de la mirada.
2. Sostener la regla milimetrada verticalmente, cerca del ojo abierto del paciente, para medir la distancia entre el centro de los márgenes palpebrales superior e inferior.
3. Registrar la altura de la fisura interpalpebral en milímetros para cada ojo.
4. Chequear las mediciones, y además obtener las siguientes mediciones:
· Distancia entre el margen del párpado superior y el reflejo corneal (normalmente 4mm).
· Distancia entre el margen del párpado inferior y el reflejo corneal (normalmente 6mm aprox.).
Distancia entre el margen del párpado superior y el reflejo corneal
1. Sostener la luz de la linterna directamente frente al paciente, de tal manera que quede la mirada en posición primaria y se pueda observar el reflejo corneal.
2. Usar una regla milimetrada para medir la distancia entre el centro del margen del párpado superior y el reflejo corneal.
3. Registrar la distancia para cada ojo, usar números negativos si el párpado ocluye el reflejo corneal.
4. Registrar la posición del pliegue del párpado superior de cada ojo. Observar si el pliegue del párpado está ausente o no puede ser medido exactamente.
Función del Elevador
1. Colocar el pulgar o la palma de la mano sobre la frente del paciente. Esta maniobra previene que el músculo frontal asista al elevador del párpado, lo que permitirá valorar la función del elevador.
2. Pedir al paciente que mire hacia abajo, colocar el cero de la regla sobre el borde del párpado superior, sin tocar las pestañas.
3. Sin mover la regla, pedir al paciente que mire al frente hacia un punto lejano. Mantener la regla fija, medir la nueva localización del borde del párpado. La diferencia entre las dos mediciones (la cantidad total de excursión del elevador) nos da la función del elevador.
4. Registrar la función del elevador para cada ojo en milímetros.
Posición del pliegue de la belleza
1. Colocar el pulgar o la palma de la mano sobre la frente del paciente. Esta maniobra previene que el músculo frontal asista al elevador del párpado, lo que permitirá valorar la función del elevador.
2. Medir la distancia entre el margen del parpado superior y el pliegue de la belleza.
3. Registrar la posición del pliegue de la belleza en cada ojo. Anotar si el pliegue de la belleza esta ausente o si no se puede medir adecuadamente.
Procedimiento:
1) Enfocar el ocular del queratómetro.
2) Ajustar la mentonera del paciente en el aparato correctamente.
3) Ajustar altura del aparato al paciente y decirle al paciente que no lleve ni gafas ni lentes de contacto en la prueba.
4) Decirle al paciente que mantenga fija la mirada al infinito y alineamos las miras del queratómetro .
5) Con el joystick alineamos el círculo pequeño con el círculo inferior derecho.
6) Alinear los signos ‘+‘ y signos ‘ – ‘ de forma ‘exacta’.
7) Para la medición horizontal, hay que superponer los 2 signos ‘ – ‘ .
8) Para la medición vertical, superponemos los signos ‘ + ‘ .
Pruebas lagrimales
BUT
Previa instilación de fluoresceína mediante el ligero contacto en la conjuntiva inferior de una tira de fluoresceína (Barnes Hind® Ful-Glo® Fluorescein Sodium Ophthalmic Strip) humectada con una gota de solución salina (Sensitive eyes® plus Baush & Lomb®) se determinó el BUT contando el tiempo transcurrido entre el último parpadeo y la formación del primer punto o línea oscura indicativo de la rotura lagrimal. Cuando el tiempo de rotura superaba los 50 seg se interrumpía la prueba y se contabilizaba como 51. Para ello el paciente se situó en la mentonera de una lámpara de hendidura Shin-Nippon®. Se le pidió que parpadeara 3 veces y que mantuviera el ojo abierto tanto tiempo como fuera posible. La iluminación fue moderada y se utilizó el filtro azul-cobalto junto con el filtro amarillo Wratten n.º 12 con un haz ancho, ya que se ha encontrado que el uso de una sección óptica con posterior escaneo de la córnea, aunque facilita la determinación del BUT, produce valores erróneamente elevados (11). Se tomaron 3 valores de BUT y se promediaron los 2 más cercanos (16).
NIBUT
La medida del NIBUT se realizó con el instrumento Tearscope® (Keeler Ltd, Windsor, Berkshire) junto con el sistema de magnificación de una lámpara de hendidura Shin-Nippon®. Se situó un test de rejilla en el Tearscope® y se pidió al paciente, bien situado en la mentonera, que parpadeara 3 veces y que mantuviera el ojo abierto tanto tiempo como fuera posible mientras fijaba en el centro de la rejilla. La iluminación fue moderada y la magnificación 10 X. Se tomaron 5 valores de NIBUT y se promediaron los 3 más cercanos (13,16).
Para mantener las mismas condiciones de humedad y temperatura todas las medidas se realizaron en un mismo gabinete, y para evitar que el lagrimeo reflejo interfiriese en los resultados se esperó como mínimo 5 minutos entre cada técnica. Debido a su naturaleza invasiva, el BUT siempre se determinó después del NIBUT.
Prueba de shimerr
La prueba de Schirmer es una prueba que determina si el ojo produce suficientes lágrimas para mantenerlo húmedo.
El proveedor de atención médica colocará la punta de una tira especial de papel dentro del párpado inferior de cada ojo. Ambos ojos se examinan al mismo tiempo. Antes del examen, le aplicarán gotas oftálmicas anestésicas con el fin de evitar el lagrimeo de los ojos, debido a la irritación causada por las tiras de papel.
El procedimiento exacto puede variar. La mayoría de las veces, los ojos se cierran durante 5 minutos. Cierre los ojos suavemente, ya que el hecho de frotarse los ojos o apretar al cerrarlos durante la prueba puede arrojar resultados anormales del examen.
Después de 5 minutos, el médico retira el papel y mide qué tanto del papel está húmedo.
Algunas veces, el examen se hace sin gotas anestésicas para buscar otros tipos de problemas de lagrimeo.
El examen con hebra de hilo impregnada de rojo de fenol es similar a la prueba de Schirmer, sólo que se utilizan tiras rojas de un hilo especial en lugar de las tiras de papel. No se necesitan gotas anestésicas. El examen demora 15 segundos.
Cuestionario McMonnies, Cuestionario OSDI
El comité de ética de la facultad de medicina de la Universidad de Valladolid autorizó, financió y repasó todos los procedimientos requeridos para la realización del presente estudio. Se seleccionaron, al azar, pacientes mayores de 50 años del sistema de salud de Castilla y León en Valladolid. Tras su elección, éstos firmaron un consentimiento informado que explicaba la finalidad y procedimientos del estudio. Respondieron a dos cuestionarios validados para la evaluación de los síntomas del SOS y se les realizó una exploración oftalmológica completa.
El primer cuestionario (Q1) es la versión modificada del McMonnies dry eye index y el cuestionario 2 (Q2) correspondió al OSDI, ambos traducidos al castellano4. Q1 fue realizado en la práctica de medicina general y se componía de 8 preguntas dicótomas (sí=1 / no=0). éstas incluían preguntas relacionadas con la sensación de ardor, arenillas, ojo rojo, secreciones matutinas, frecuencia de infecciones oculares, uso de lágrimas artificiales, molestias en ambientes secos y dificultad para deglutir sin beber agua. Q2 consistió en 12 preguntas sobre síntomas relacionados con el ojo seco y la frecuencia de cada una de ellos. Se preguntó sobre fotofobia, sensación de arenilla, dolor o ardor, visión borrosa, disminución de la agudeza visual, dificultades con la lectura, conducción nocturna, viendo televisión o utilizando el ordenador, molestias con el viento, ambientes secos o aire acondicionado. Además, a cada síntoma se le asignó un valor de frecuencia dentro de la escala del 0 al 5, donde un 0 equivalía a "nunca", 1 a "ocasionalmente", 2 a "a veces", 3 a "la mitad del día, 4 a "la mayoría del día" y 5 a "siempre". Un oftalmólogo entrenado realizó las siguientes pruebas diagnósticas: tinción corneal (- / +) con tiras de fluoresceína (Laboratoire Chauvin, Aubenas, France), tinción corneal o conjuntival (- / +, clasificación Oxford) con tiras de Rosa de Bengala (RB) (Akorn, Inc. Buffalo Grove, IL, USA), tiempo de ruptura lagrimal (TBUT, >10 segundos=normal o <10 segundos=patológico) y la prueba de Schirmer con anestesia (5 minutos, > 5 mm=normal o < 5mm=patológico). La combinación de TBUT, como prueba altamente sensible, junto con la prueba de Schirmer, por su alta especificidad, fue seleccionada como nuestra prueba clínica diagnóstica principal para el SOS4-9. El análisis estadístico se realizó con el Statistical Package for the Social Sciences (SPSS; versión 12.0, SPSS Inc, Chicago, IL, USA). El análisis descriptivo para variables cualitativas se reportó en frecuencias de distribución y las cuantitativas como medias con intervalos de confianza al 95%(IC 95%). Utilizamos la prueba del Chi-cuadrado para variables cualitativas, la de la t de Student para las cuantitativas y una de las variables dicotómicas, análisis de varianza si la variable tenía más de 2 categorías y la prueba de Duncan para comparaciones múltiples. La validez de los cuestionarios fue analizada como el área bajo la curva "receiver operating characteristic" (ROC) con IC 95%, alfa de Cronbach para el análisis de consistencia interna, sensibilidad y especificidad. Los valores predeterminados para el área bajo la curva ROC se asignaron de la siguiente manera: < 0,5=sin capacidad discriminatoria para SOS; 0,7 - 0,8=discriminación aceptable; 0,8 - 0,9=buena discriminación y > 0,9=excelente discriminación.
La validez de Q1 y Q2 se midió utilizando el coeficiente de la correlación del alfa de Cronbach y los valores > 0,70 validaron la consistencia interna3. El análisis de concordancia describe la fuerza con la que variables independientes concuerdan entre si. Este análisis da como resultado el índice kappa (κ), cuyos valores indicaron: < 0,20=pobre concordancia; 0,21 - 0,40=concordancia débil; 0,41 - 0,60=concordancia moderada; 0,61 - 0,80=buena concordancia; 0,81 - 1,00=muy buena concordancia. Valores de p<0,05 se consideraron estadísticamente significativos.
Resultados
Un total de 270 sujetos (58,2% mujeres; 41,8% hombres) con edad promedio de 64,5 años (IC 95%: 63,3 - 65,7) se enrolaron. El rango de puntuación para Q1 fue de 0 (sin síntomas) a 6 y la media fue de 1,2; la mayoría de los pacientes tuvieron al menos un síntoma. El rango de la prevalencia del SOS para Q1 varió entre 2,6% para "dificultad para tragar sin agua" a 33% para "sensación de arenillas" (tabla 1). La "sensación de arenillas" y las "molestias en ambientes secos" (28,9%) fueron los síntomas más frecuentes registrados en Q1. El promedio de valores de sensibilidad para Q1 fue de 14% para "ojos rojos" a 33,3% para "dificultad para tragar sin agua".
El rango de valores para la especificidad de Q1 fue de entre 73,4% para "ojos rojos" a 77,5% para "sensación de arenillas".
El rango de puntuaciones para la frecuencia de cada síntoma de Q2 fue de 0 para "nunca tengo síntomas" a 5 para "siempre tengo síntomas", excepto por el ítem "dificultad al utilizar el ordenador" donde se registró una máxima puntuación de 3 ("síntomas la mitad del día").
Los resultados de los síntomas más comúnmente manifestados se encuentran en la tabla 2 y destacamos "sensación de arenillas" (99,2%) y "sensación de ardor" (98,9%). La media del promedio para la frecuencia de síntomas en Q2 fue de 1,4 (rango 1 - 3,63) y la mayoría de los pacientes respondió que presentaban síntomas de SOS "a veces" o menos.